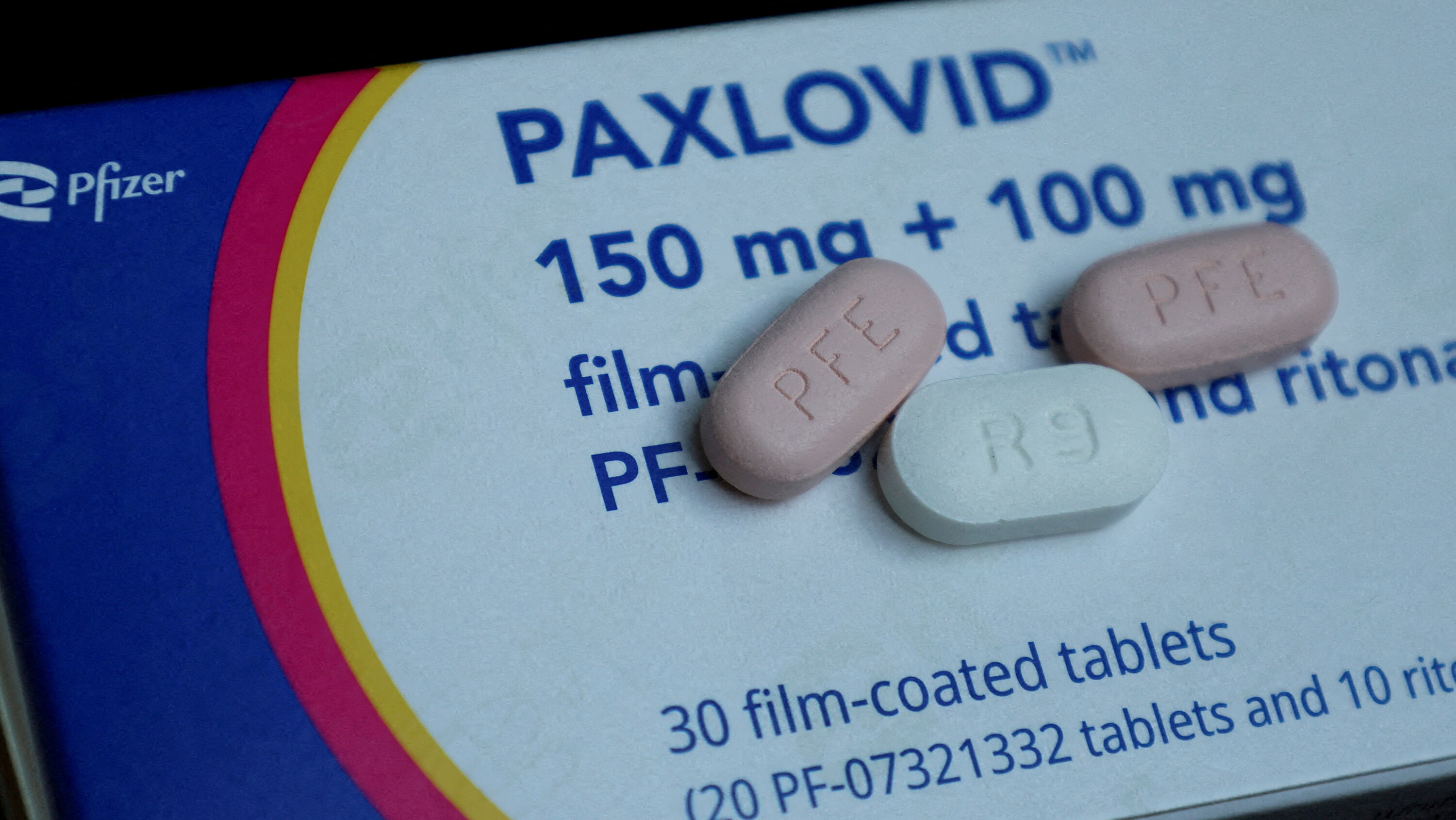
El suministro del medicamento debe realizarse bajo estricta vigilancia médica.
La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) ha aprobado el registro sanitario de Paxlovid (nirmatrelvir/ritonavir), del laboratorio Pfizer.
Este medicamento está destinado a tratar Covid-19 en adultos que no requieren oxígeno suplementario pero que presentan un mayor riesgo de desarrollar una forma grave de la enfermedad.
Tras la evaluación del Comité de Moléculas Nuevas (CMN) y el análisis técnico del equipo especializado de Cofepris, se autorizó la venta de Paxlovid como el primer medicamento aprobado para prevenir hospitalizaciones y muertes relacionadas con Covid-19.
El medicamento cumple con los requisitos de calidad, seguridad y eficacia según la información del expediente técnico. Este medicamento ya cuenta con la aprobación de autoridades internacionales como la FDA en EE. UU., Health Canada, la EMA en Europa, así como la Agencia Nacional de Vigilancia Sanitaria de Brasil (Anvisa) y la Agencia Nacional de Medicamentos de Chile (Anamed).
Cabe mencionar, que para adquirir Paxlovid, es necesaria una prescripción médica. Cofepris enfatizó que los profesionales de la salud deben considerar cuidadosamente los factores de uso y riesgo para evitar el mal uso y la automedicación. El suministro del medicamento debe realizarse bajo estricta vigilancia médica.
Noticias que podrían interesarte:
- Precio del dólar hoy 4 de mayo de 2026 en México: tipo de cambio y bancos
- Simulacro Nacional 2026: hora de la alerta sísmica y qué hacer paso a paso
- Pemex elimina Gasolinas Bienestar: qué cambia en la venta de petróleo a Cuba
- Onda de calor golpea México este 4 de mayo: hasta 45 grados, lluvias y vientos fuertes
- Precio del dólar hoy 5 de mayo de 2026 en México: tipo de cambio y bancos