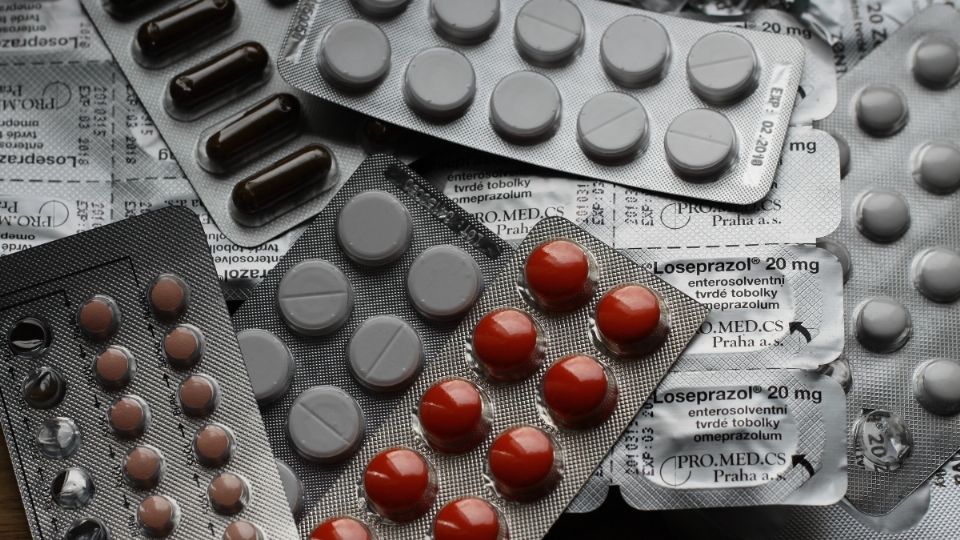
Ciudad de México.- Después de mucho esfuerzo del equipo técnico y científico de Cofepris, se logró autorizar la comercialización de más de 1.4 millones de cajas de medicamentos psiquiátricos. Ante las irregularidades del fabricante, la autoridad creó una ruta regulatoria garantizando que los medicamentos disponibles son seguros, eficaces y de calidad.
Se trata de 69 lotes de medicamentos de atención psiquiátrica producidos por Psicofarma que aprobaron un riguroso análisis técnico, cumpliendo el compromiso de garantizar el acceso a medicamentos controlados seguros, eficaces y de calidad.
Después de graves irregularidades encontradas al fabricante farmacéutico y hechas públicas en la Carta de Hallazgos, de manera proactiva esta autoridad sanitaria trazó una ruta regulatoria que promoviera avanzar en el acceso a medicamentos de atención psiquiátrica. Por ello, de manera transparente brindó acompañamiento a la empresa para que entregara la documentación y las pruebas requeridas.
Hasta el momento, el fabricante ha comprobado que 69 lotes de medicamentos cumplen las pruebas determinadas por la farmacopea de los Estados Unidos Mexicanos, y se tiene la certeza de que no representan un riesgo a la salud. Y a razón de seguir el principio de “liberación útil para el abasto nacional”, la autorización otorgada establece que podrán liberarse únicamente para el mercado nacional.
El equipo de dictaminadores especializados dedicados al análisis de los medicamentos del fabricante concluyó que el resto de los lotes presentados a evaluación no contaron con las condiciones para cumplir los estándares de seguridad, calidad y eficacia para prevenir riesgos a la salud de las y los pacientes.
Se da a conocer que la comercialización de los fármacos será totalmente responsabilidad de la empresa y que inmediatamente después de la liberación de aproximadamente un millón 403 mil 693 cajas de clonazepam, litio, metilfenidato y metilfenidato liberación prolongada, estos medicamentos serán sujetos a un esquema de farmacovigilancia intensiva en apego al numeral 7.7.1. de la NOM- 220-SSA 2016, que garantizará la detección de posibles eventos adversos asociados a su uso.
Noticias que podrían interesarte:
- Registro obligatorio de celulares en México: así puedes evitar quedarte sin servicio en 2026
- Precio del dólar HOY 11 de abril de 2026 en México: así amanece el tipo de cambio y lo que debes saber
- Sarampión en México supera 15 mil casos y enciende alertas por impacto en niños pequeños
- Nueva regla de telefonía en México: quiénes se salvan del registro con CURP y qué pasa si no cumples
- Clima hoy en México 11 de abril: lluvias intensas, calor extremo y alerta por vientos peligrosos